
Avis de l’Ordre des psychologues du Québec
Depuis l’adoption de la loi 22, l’évaluation des troubles neuropsychologiques est une activité réservée exclusivement au psychologue, dans le cadre de son champ d’exercice lorsqu’une attestation de formation lui est délivrée par l’Ordre des psychologues du Québec, de même qu’aux médecins. Ainsi, l’utilisation du Dépistage Cognitif de Québec (DCQ) ne saurait servir d’autres fins que celles du dépistage. C’est un outil qui pourrait aussi être utilisé par différents professionnels pour apprécier, soit relever et prendre en considération des manifestations cliniques ou des difficultés, et ce, pour tirer des conclusions relatives à leur champ d’exercice propre. Dans ces cas, il ne s’agirait pas d’apprécier aux fins d’apprécier seulement. Cette appréciation se situerait dans le cadre des évaluations que permettent chacun des champs d’exercice des différents professionnels. Pour ne prendre que quelques exemples, les ergothérapeutes se serviraient des difficultés relevées à l’aide du DCQ pour conclure sur les habiletés fonctionnelles et les travailleurs sociaux feraient de même, mais pour conclure sur le fonctionnement social.
Ordre des psychologues du Québec
Remerciements
Sincères remerciements à Patrick Bégin, mon ami d’enfance, qui a toujours été versatile sur la planche à dessin et qui a su représenter les mises en situations du DCQ avec tout son talent. Merci aussi à la Fondation du CHU de Québec, à Novartis, au CIRTMC et à la Société Alzheimer de Québec pour leur appui financier tout au long de ce projet. Merci à tous mes collègues qui ont collaboré à la validation du DCQ notamment Audrey Paradis, David Bergeron, Anne-Marie Cayer, Justine de la Sablonnière, Kim Hoang Trinh, et Antoine Vermette.
À propos des auteurs
Laforce RJr
Dr Robert Jr Laforce est médecin spécialisé en neurologie cognitive et neuropsychologue clinique. Il est Professeur Agrégé de Neurologie et Co-responsable du cours de Neurologie à la Faculté de médecine de l’Université Laval. Il est l’instigateur principal du Dépistage Cognitif de Québec (DCQ). Il est aussi impliqué dans plusieurs projets de recherche sur les démences atypiques notamment l’effort international GENFI (Genetic Frontotemporal Dementia Initiative) subventionné par les IRSC et le Weston Brain Institute. Il a plus d’une cinquantaine de publications scientifiques dans des journaux revus par les pairs et de multiples chapitres de livre. Il est particulièrement intéressé par les démences frontotemporales. À ce sujet, il a complété un Fellowship dans ce domaine à l’Université de Californie à San Francisco, au Memory and Aging Center et continue de collaborer avec plusieurs chercheurs internationaux dans le domaine des démences.
Sellami L
Dre Leila Sellami est une neurologue de Tunisie actuellement en Fellowship à la Clinique Interdisciplinaire de Mémoire (CIME) dans notre programme de Fellowship en Neurologie Comportementale et Neuropsychiatrie.
Bergeron D
David Bergeron est un étudiant au MD-PhD à l’Université Laval. Il complète actuellement son doctorat sur le diagnostic des démences atypiques à la CIME sous la supervision du Dr Laforce.
Verret L
Dr Louis Verret est le co-directeur du Volet Neurologique de la CIME. Il a complété ses études à l’Université Laval, puis a réalisé un Fellowship en neurologie comportementale à l’Université McGill, à Montréal. Il s’implique dans l’enseignement, collabore à plusieurs projets de recherche, et dirige la majorité des essais cliniques à la CIME.
Fortin MP
Co-directrice du Volet Gériatrique de la CIME, le Dre Marie-Pierre Fortin collabore à plusieurs projets de recherche. Elle a complété sa formation en gériatrie à l’Université Laval avant de réaliser un Fellowship en troubles cognitifs à Lyon, en France. Elle est également diplômée du programme de neuropsychologie clinique de l’Université de Montpellier en France.
Houde M
Dre Michèle Houde a réalisé une maîtrise en science avant d’entreprendre ses études en médecine à l’Université Laval. Intéressée autant par la neurologie que la psychiatrie, elle a fait une formation en psychiatrie puis en gérontopsychiatrie. Elle détient un Fellowship en neurologie comportementale réalisé à l’hôpital Juif de Montréal.
Roy M
Dans le cadre de son travail d’assistant de recherche, M. Roy a contribué à l’élaboration de quelques-unes des tâches du DCQ.
Poulin S
Co-directeur du programme de surspécialité en neurologie comportementale et neuropsychiatrie (fellowship), le Dr Stéphane Poulin est très impliqué dans l'enseignement et la recherche. Il a complété ses études de médecine en psychiatrie avant de se surspécialiser aux McLean Hospital et Massachussetts General Hospital (Harvard Medical School).
Macoir J
Dr Joël Macoir est Orthophoniste et Professeur Titulaire au Département de Réadaptation de la Faculté de médecine, Université Laval. Il est également chercheur dans le Centre de recherche de l'Institut universitaire en santé mentale de Québec. Il est l’auteur de nombreuses publications et chapitres de livre. Dr Macoir mène plusieurs projets de recherche sur les aphasies primaires progressives.
Hudon C
Dr Carol Hudon détient un doctorat en psychologie de la faculté des sciences sociales de l’Université Laval et a réalisé un stage postdoctoral à l’Institut universitaire de gériatrie de Montréal. Il est professeur titulaire neuropsychologie à l’École de psychologie de l’Université Laval. Les neurosciences cliniques et cognitives sont ses principaux champs de recherche.
Bouchard RW
Dr Rémi W. Bouchard est le fondateur de la Clinique interdisciplinaire de mémoire (CIME). Il a complété son doctorat en médecine ainsi qu’une maîtrise en neurobiologie à l’Université Laval avant d’entreprendre une formation en neurologie cognitive et comportementale au Boston City Hospital de l’Université d’Harvard ainsi qu’un Fellowship à l’Hôpital de la Salpêtrière de Paris. Il est le leader Québécois incontesté de l’évaluation clinique des troubles cognitifs et s’implique activement dans l’enseignement, la recherche et les publications scientifiques.
Message des auteurs
Il est recommandé de suivre une formation avant d’administrer le DCQ sur une base régulière dans un contexte de dépistage clinique. Nous croyons que ceci améliorera la qualité de l’acte en favorisant une administration standardisée et une interprétation qui respecte les limites de l’instrument. Des formations sont disponibles sur une base périodique; renseignez-vous à dcqtest@gmail.com
Introduction
De nos jours, à la grandeur de l’Amérique, une personne développe une démence toutes les 68 secondes… Il est estimé qu’en 2050, il y aura un nouveau cas toutes les 33 secondes… De ce fait, les démences représentent une source majeure d’invalidité et d’institutionnalisation et posent une menace à la santé publique.
Plusieurs outils sont actuellement disponibles pour aider au dépistage et au diagnostic des maladies cognitives. Bien que ces outils aient démontré leur efficacité au fil du temps, ils présentent quelques lacunes puisqu’ils ne ciblent pas tous les aspects cognitifs des démences atypiques notamment et aucun ne comporte d’échelle comportementale.
Contrairement aux démences typiques (ex: la maladie d’Alzheimer dans sa variante amnésique, le trouble cognitif vasculaire), le délai entre l’apparition des symptômes et le diagnostic des démences atypiques (ex: variantes langagière, visuelle ou frontale/dysexécutive de la maladie d’Alzheimer, aphasies primaires progressives, et le spectre des démences frontotemporales) peut atteindre jusqu’à cinq ans, retardant significativement la prise en charge et le traitement, augmentant ainsi le fardeau sur le système de santé. Cette situation indésirable est principalement due au sous-diagnostic des démences, notamment en l’absence d’outil de dépistage adapté aux nouveaux critères actualisés (Gorno-Tempini et al., 2011; McKhann et al., 2011; Rascovsky et al., 2011).
Le DCQ est un outil de dépistage actualisé en fonctions des nouveaux critères de démence, validé sur 400 sujets normaux âgés entre 50 et 85 ans. Il s’administre en 25 minutes. Il corrèle fortement avec le Montreal Cognitive Assessment (MoCA), mais ses 5 index (Mémoire, Visuospatial, Exécutif, Langage, Comportemental) permettent une administration à la carte afin d’aller plus loin dans un domaine ciblé par le clinicien (voir Figure 1).

Figure 1. Résumé des index du DCQ.
La place du DCQ dans le dépistage cognitif demeure à préciser (voir Figure 2). Nous croyons que le DCQ ne remplacera jamais l’exploration diagnostique approfondie que représente l’évaluation neuropsychologique qui elle demeure le standard de pratique requis dans certaines circonstances bien ciblées. Nous croyons plutôt que le DCQ est une étape cruciale vers une meilleure reconnaissance des démences, une diminution du délai de prise en charge, un traitement ciblé et une utilisation plus efficace des ressources en santé. Le temps saura préciser sa véritable pertinence…
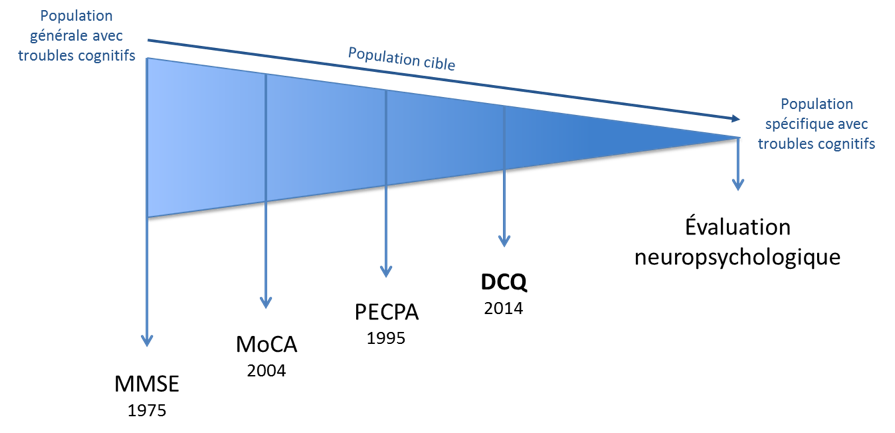
Figure 2. La place du DCQ dans le dépistage cognitif.
Bonne lecture!
2. Brève revue des démences
À l’échelle mondiale, les démences représentent une source importante d’invalidité et d’institutionnalisation chez les personnes âgées et elles posent actuellement une menace significative à la santé publique. Selon le World Alzheimer Report, le nombre de gens atteints de démence s’élèverait à 35,6 millions, et ce chiffre augmentera à 115,4 millions d’ici 2050 si un traitement convenable n’est pas instauré (Wimo and Prince, 2010). Selon une étude canadienne sur la santé et le vieillissement, près de 8 % de la population canadienne âgée de 65 ans et plus souffre de démence (Gauthier et al., 1990). Ainsi, l’âge représente un facteur de risque important puisque la probabilité de développer une démence augmente de 2,4 % entre 65-74 ans à 34,5 % chez les 85 ans et plus. Cet effet est considérable puisque le nombre de personnes âgées de plus de 65 ans atteindra 21 % de la population d’ici 2026. Les coûts rattachés aux démences se calculant en milliards, ces dernières sont désormais considérées comme une épidémie silencieuse (Bergman et al., 2009; Hurd et al., 2013).
Les causes de démence
Près de 80 % des cas sont causés par la maladie d’Alzheimer (MA) et le trouble cognitif vasculaire (TCV), alors que 20 % sont attribuables au spectre des démences frontotemporales (Ratnavalli et al., 2002; Kelley et al., 2008; Rossor et al., 2010; Laforce et al., 2015).
Les démences typiques versus démences atypiques (Voir Tableau 1)
Une démence dite « typique » est reconnaissable par son profil épidémiologique, cognitif, et radiologique. La variante amnésique de la MA, par exemple, est reconnue par son impact sur la mémoire épisodique et les atteintes fonctionnelles qui en découlent. Elle débute généralement par un trouble cognitif léger amnésique (Petersen et al., 2005; Petersen et al., 2009) où l’individu rapporte des pertes de mémoire, notées par les proches, qui n’interfèrent pas avec le fonctionnement quotidien. Ceci progresse en s’étendant aux habiletés exécutives avant d’affecter les activités quotidiennes. Le taux de conversion en MA est de 15 % par année (Petersen et al., 2005; Tabert et al., 2006; Zanetti et al., 2006).
À l’inverse, une démence est « atypique » lorsqu’elle se caractérise par des atteintes principalement non mnésiques chez des individus plus jeunes. L’âge moyen des personnes touchées est de 60 ans (Galton et al., 2000; Gorno-Tempini et al., 2004; Renner et al., 2004; Tang-Wai et al., 2004; Frisoni et al., 2007; Migliaccio et al., 2009; Rabinovici and Miller, 2010). Les démences atypiques se distinguent souvent par des troubles langagiers, visuospatiaux ou comportementaux. Ces cas peuvent aussi combiner un trouble neurologique moteur (rigidité, lenteur à la marche). Alors que d’autres peuvent présenter des changements comportementaux comme de l’apathie, une désinhibition, des altérations des habitudes alimentaires, ou des hallucinations au premier plan (Boeve and Graff-Radford, 2012; Mahoney et al., 2012; Snowden et al., 2013). Récemment, l’intérêt pour les démences atypiques a sensiblement augmenté, ce qui a contribué à la révision des critères du National Institute of Neurological and Communicative Disorders and Stroke-Alzheimer's Disease and Related Disorders Association (McKhann et al., 2011). Ces critères avaient une sensibilité de 80 % et une spécificité de 70 % comparativement à l’examen pathologique (Knopman et al., 2001). Ils nécessitaient absolument un trouble de mémoire comme problème principal et ne tenaient pas compte des biomarqueurs génétiques, structurels, et moléculaires. La reconnaissance du trouble cognitif léger non amnésique (Petersen et al., 2009), la publication de critères sur la MA qui tiennent compte des variantes non amnésiques (McKhann et al., 2011), de critères sur la variante comportementale de la démence frontotemporale (Rascovsky et al., 2011) et des aphasies primaire progressives (Gorno-Tempini et al., 2011) permettront de promouvoir une meilleure détection de ces maladies.
Démences typiques
(80% des cas)
- La variante amnésique de la maladie d’Alzheimer (McKhann et al., 2011)
- Le trouble cognitif vasculaire (Gorelick et al., 2011)
- La démence à corps de Lewy (McKeith et al., 2005)
Démences atypiques
(20% des cas)
-
Les aphasies primaires progressives
- La variante sémantique (Gorno-Tempini et al., 2004; Gorno-Tempini et al., 2011; Snowden et al., 2013)
- La variante agrammatique/non fluide (Gorno-Tempini et al., 2004; Gorno-Tempini et al., 2011; Grossman, 2012)
- La variante comportementale de la démence frontotemporale (Rascovsky et al., 2011)
- L’apraxie primaire de la parole (Josephs et al., 2012)
- Le syndrome corticobasal (Lee et al., 2011)
-
Les variantes de la maladie d’Alzheimer
- La variante visuelle (aussi appelée atrophie corticale postérieure) (Migliaccio et al., 2009; McKhann et al., 2011)
- La variante langagière (aussi appelée logopénique) (Gorno-Tempini et al., 2004; Gorno-Tempini et al., 2011)
- La variante comportementale/dysexécutive (Mendez et al., 2013; Ossenkoppele et al., 2015)
Tableau 1. Les types de démences
3. Le dépistage cognitif
La démence est un diagnostic clinique qui repose sur l’histoire telle que rapportée par le patient et corroborée par un proche, l’examen neurologique, le dépistage cognitif (Mini-Mental State Examination – Folstein et al., 1975; Montreal Cognitive Assessment – Nasreddine 2005), des tests sanguins (formule sanguine, ions, thyroïde, vitamine B12) et l’imagerie cérébrale (afin d’éliminer une cause réversible, telle une tumeur) (Gauthier et al., 2012) Bien qu’elles présentent des caractéristiques fort distinctes des démences typiques, aucun guide de pratique n’a été développé pour la détection précoce et la prise en charge des démences atypiques si bien que leur identification repose souvent sur une surspécialisation médicale. Inévitablement, la détection est sous-optimale particulièrement en 1re ligne. Considérant que la pathologie principale qui sous-tend les variantes atypiques est souvent similaire à la MA, et que nous disposons d’un traitement, il est inconcevable que ces cas ne soient pas dépistés plus tôt.
Ce qui est particulièrement problématique est qu’il n’existe pas d’outils fiables qui soient conçus spécifiquement pour dépister les démences atypiques en médecine de 1ère ligne. Les outils qui ont été développés pour le dépistage des démences typiques ne sont aucunement adaptés aux démences atypiques. Près de 60 % des démences atypiques seraient manquées (faux négatifs) avec les instruments de dépistages actuels (Appels and Scherder, 2010). Ces tests comportent également plusieurs lacunes.
Le Mini-Mental State Examination (MMSE; Folstein 1975)
Depuis sa publication en 1975, le Mini-Mental State Examination (MMSE; (Folstein et al., 1975) git en tant qu’outil de 1ière ligne dans le dépistage des troubles cognitifs. Ses qualités tiennent dans le fait qu’il est facile à administrer, qu’il procure un aperçu général des fonctions cognitives en s’administrant en près de 10 minutes et qu’il permet souvent d’identifier une démence modérée à sévère. Depuis quelques années cependant, la sensibilité et la spécificité du MMSE ont été remises en question particulièrement en raison de son niveau de difficulté relativement restreint et du fait qu’il est peu utile pour le diagnostic des démences lorsque la prévalence est sous le seuil des 60%.
Par ailleurs, cet outil ne permet pas un dépistage aussi sensible que d’autres instruments dans la détection du trouble cognitif léger, cette zone de transition entre le vieillissement normal et la démence. Le score attribué à la mémoire ne tient pas compte de la différence rappel libre/indicé, une distinction cruciale dans le diagnostic différentiel de la MA selon les nouveaux critères (McKhann et al., 2011). Le MMSE ne mesure pas la composante comportementale souvent altérée dans les démences atypiques. Plusieurs travaux ont démontré que même si le MMSE est l’instrument le plus utilisé dans l’évaluation cognitive des patients atteints de la maladie de Parkinson par exemple, sa précision et sa sensibilité à détecter les troubles cognitifs chez ces patients sont faibles (Nazem et al., 2009). Enfin, le MMSE ne permet pas de détecter adéquatement les troubles cognitifs chez les patients très scolarisés.
Le Montreal Cognitive Assessment (MoCA; Nasreddine 2005)
Récemment, de nombreuses recherches ont montré que le Montreal Cognitive Assessment (MoCA; (Nasreddine et al., 2005) possède de meilleures qualités psychométriques en tant qu’instrument de dépistage du trouble cognitif léger ou de la MA dans la population générale (Nasreddine et al., 2005), la maladie de Parkinson (Hoops et al., 2009) ou encore le trouble cognitif vasculaire (Dong et al., 2010). La présence de sous-tests mesurant les fonctions exécutives (exemples: la fluidité verbale, la mémoire de travail) sont probablement à la base de ce qui fait que le MoCA est un instrument supérieur au MMSE.
À l’heure actuelle, il représente l’outil de première ligne idéal pour le dépistage du trouble cognitif léger et des démences. Cependant, tout clinicien expérimenté œuvrant dans une clinique spécialisée de démence, où les cas référés sont souvent très complexes et multifactoriels, peut affirmer que même si le MoCA possède des qualités supérieures au MMSE, il présente de nombreuses lacunes sur le plan de l’évaluation cognitive. Par exemple, le sous-test du Trail Making comporte peu d’items. L’horloge et le cube doivent être dessinés dans un espace très restreint et la correction de l’horloge est très sévère. Conséquemment, les formes corticales postérieures de la MA sont moins à risque d’être dépistées (McKhann et al., 2011). Le sous-test de dénomination, quant à lui, ne comporte que 3 items qui s’avèrent peu sensibles et peu spécifiques pour la détection d’un trouble du langage puisque ces items ne permettent pas de bien circonscrire un trouble du langage associé aux nouvelles formes de démences récemment décrites (ex: la forme logopénique de la MA; (Gorno-Tempini et al., 2011)). La mémoire verbale est bien évaluée mais aucun item mesurant la mémoire visuelle n’est inclus. De plus, le score final ne tient pas compte de la distinction entre la performance au rappel libre et la reconnaissance, démasquant ainsi les vrais déficits en mémoire épisodique, un élément clé dans le diagnostic différentiel selon les nouveaux critères (McKhann et al., 2011).
Dans le contexte où le MoCA est utilisé comme outil de dépistage populationnel du trouble cognitif dans le bureau d’un omnipraticien, ces failles ne représentent pas un problème significatif. Au contraire, l’utilisation du MoCA dans ce contexte représente une avancée par rapport au MMSE. Cependant, dans les Cliniques de mémoire de 2ième et 3ième lignes où le dépistage doit être davantage centré sur un diagnostic différentiel élaboré, le MoCA dans sa forme actuelle est souvent insuffisant. De plus, la consultation en neuropsychologie (qui représente un examen cognitif poussé de 3-6 heures) ne s’applique pas pour tous les cas, les ressources dans ce domaine sont souvent limitées et l’évaluation indument prolongée.
Le Protocole d’Examen Cognitif de la Personne Âgée (PECPA; (Geneau and Taillefer; von Gunten et al., 2006))
Le PECPA est bien connu des Ergothérapeutes québécois qui l’utilisent tant en milieu hospitalier qu’en pratique privée. Développé dans les années 90, il est utilisé chez les personnes âgées souffrant d’un syndrome cérébral organique pour le dépistage et l’identification des déficits cognitifs d’ordre légers. Il peut également aider au suivi des patients.
Le PECPA comprend un MMSE révisé ainsi que 10 sous-tests, évaluant plusieurs fonctions cognitives telles que l’orientation spatiale, la mémoire récente et ancienne et le jugement. Certains items de ce test sont sujets à générer une interférence en mémoire. À l’instar du MMSE et du MoCA, le PECPA n’a pas été développé en fonction des critères actualisés de démence et ne comporte pas d’indice comportemental.
4. Rationnel et application du DCQ
A. Rationnel du DCQ
Le DCQ a été développé à la Clinique Interdisciplinaire de Mémoire (CIME) du Centre Hospitalier Universitaire (CHU) de Québec, la plus vieille clinique de la mémoire au Canada, par un groupe d’experts en neurologie comportementale, en orthophonie et en neuropsychologie. Le DCQ est un test de dépistage cognitif qui permet d’évaluer cinq domaines (Mémoire, Visuospatial, Exécutif, Langage, Comportement) (voir Figure 1).
L’Index Mémoire comprend l’évaluation de la mémoire de travail grâce à un empan direct, un rappel immédiat de 8 mots avec un rappel différé, après une période de 15 minutes, puis une tâche de reconnaissance. L’Index Visuospatial comprend des tests de détection de forme, de rotation perceptuelle ainsi que la construction d’une figure géométrique complexe. L’Index Exécutif implique un sous-test d’empan à rebours et exige de réciter les mois à rebours. Il est également composé d’une séquence graphique, d’une tâche d’abstraction, de fluidité verbale ainsi qu’une version modifiée du Stroop. Quant à l’Index Langage, il comporte la description d’une scène, une tâche de dénomination et d’écriture, la description écrite d’une scène ainsi que des tests de compréhension, de fluidité sémantique et de répétition. Finalement, l’Index Comportemental permet d’évaluer 10 domaines: la dépression, l’anxiété, la désillusion, les hallucinations, l’irritabilité et l’agressivité, l’apathie, la désinhibition et le manque de jugement, l’obsession et la compulsion, la perte d’empathie et de sympathie puis la capacité d’autocritique (voir Figure 1). Basé sur les critères actualisés des démences, l’objectif principal du DCQ consiste donc à améliorer le dépistage des démences, typiques et atypiques, via l’administration à la carte de sous-tests spécifiquement conçus pour explorer certaines habiletés cognitives.
Pourquoi faire le DCQ plutôt que le MMSE, le MoCA ou le PECPA?
Cette décision vous appartient en tant que clinicien. Dépendamment du cadre clinique dans lequel vous travaillez, le DCQ peut s’appliquer ou non. Si votre patient est revu en suivi et la condition cognitive est claire, il n’y a aucune raison de changer de test.
Rappelez-vous que les normes du DCQ sont disponibles chez des participants normaux âgés de 50 à 85 ans.
En Clinique de mémoire spécialisée, les patients ont souvent déjà eu un MMSE et un MoCA, mais leur condition cognitive demeure néanmoins vague. Dans ces cas…
Voici trois bonnes raisons de faire le DCQ :
-
Je souhaite explorer davantage les déficits/plaintes notés au MMSE, au MoCA, au PECPA, ou à l’entrevue, et ce, dans un format à la carte en fonction de la pertinence clinique.
-
Exemple: Je note des déficits langagiers en entrevue, rapportés par la famille, mais qui ne sont pas détectés par le MoCA ou le PECPA. Je décide donc de les dépister en plus grand détail en utilisant à la carte l’Index Langage du DCQ.
Cette situation s’applique bien entendu pour tout autre domaine concerné par le DCQ (ex., Mémoire, Visuospatial, Exécutif ou Comportemental).
-
Exemple: Je note des déficits langagiers en entrevue, rapportés par la famille, mais qui ne sont pas détectés par le MoCA ou le PECPA. Je décide donc de les dépister en plus grand détail en utilisant à la carte l’Index Langage du DCQ.
- Il a été validé sur 400 sujets normaux âgés entre 50 et 85 ans et montre d’excellentes qualités psychométriques (validité et fidélité); voir (Laforce et al., soumis).
- À notre connaissance, il s’agit du premier instrument de dépistage qui ne se limite pas seulement aux domaines cognitifs classiques (Mémoire, Visuospatial, Exécutif, Langage), mais qui comporte également 10 questions spécifiques visant à dépister des changements de comportement qui peuvent faire partie du syndrome dégénératif en cause.
B. Description des sous-tests et guide de passation du DCQ
Index 1 – Mémoire (score total de 30)
Cet index comprend quatre tests qui visent à évaluer l’attention de base, la mémoire épisodique (à court et à long terme) ainsi que la mémoire de travail. Les capacités d’encodage, de consolidation ainsi que de récupération de l’information sont grandement sollicitées de la part du patient pour compléter ces épreuves. Le test permet de départager les capacités de rappel des capacités de reconnaissance du sujet.
1. Empan direct
Ce test consiste à demander au patient de répéter une série de chiffre telle que lue par l’administrateur. L’empan direct est constitué de 6 séries différentes. Il évalue l’attention de base.
Guide de passation
Administration: L’examinateur lit les séquences de chiffre au rythme d’un par seconde après avoir donné les instructions suivantes: «Je vais vous lire quelques chiffres. Écoutez attentivement et quand j’aurai terminé, répétez-les dans le même ordre. Par exemple, si je dis 8-1, vous dites…». Écrivez la réponse du sujet et cotez 0 ou 1. À la première erreur, arrêtez le test.
Cotation: Un point est alloué pour chaque séquence correctement répétée.
Score total: 6
2. Rappel immédiat
a) Encodage
Une carte constituée de 8 mots de différentes catégories est présentée au patient. Il lui est alors demandé de lire ces mots et de tenter de s’en rappeler puisqu’ils seront demandés à quelques reprises au cours du test. Une fois que le sujet a lu et mémorisé les mots, il doit indiquer quel mot appartient à la catégorie questionnée par l’examinateur et ainsi de suite, jusqu’à ce que toutes les catégories aient été questionnées.
Guide de passation
Administration: A) L’examinateur présente la carte de mot et donne les instructions suivantes: «Lisez ces mots à voix haute de haut en bas, et tentez de vous en souvenir parce que je vais vous les redemander plus tard». B) Lorsque le sujet a terminé, l’examinateur donne les instructions suivantes : «Indiquez-moi quel est l’animal?» et ainsi de suite selon la liste des catégories fournies dans le tableau du Cahier de l’examinateur.
Cotation: Aucun point n’est alloué pour l’encodage.
b) Interférence
Dans cette section, il est demandé de compter à l’envers en enlevant des tranches de 3 à partir de 97. Le patient doit donner le plus de réponses possibles à l’intérieur de 15 secondes.
Guide de passation
Administration: L’examinateur dit: «Maintenant, comptez à l’envers à partir de 97 en enlevant des tranches de 3». L’examinateur note les réponses du sujet et l’arrête après 15 secondes.
Cotation : Aucun point n’est alloué pour l’interférence.
c) Rappel immédiat
Ici la tâche consiste à demander au patient de répéter les mots qu’il a appris au début du test. Ces derniers peuvent être donnés dans n’importe quel ordre. Si le patient ne se souvient plus des mots, l’administrateur peut donner un indice de catégorie (par exemple, il peut demander quel était l’animal).
Guide de passation
Administration: L’examinateur dit: «Parmi les mots que vous venez de lire, dites-moi tous ceux dont vous vous souvenez dans n’importe quel ordre.» L’examinateur doit encercler « L » pour les rappels libres dans l’espace réservée à cet effet. Pour tous les mots non-rappelés, l’examinateur fournit un indice de catégorie, par exemple, il dit: «Quel était l’animal?» et ainsi de suite. L’examinateur encercle « I » pour tous les mots rappelés avec un indice et fait un « X » dans la colonne Ne sait pas lors d’un échec au rappel libre ou indicé. L’examinateur note l’heure de fin du rappel immédiat.
Cotation: Un point est alloué pour chaque mot rappelé librement ou avec un indice et est noté dans la colonne appropriée.
Score total: 8
3. Rappel différé
Le rappel différé permet de tester les capacités de récupération et de reconnaissance en mémoire épisodique. Il doit être administré 15 minutes après la fin du rappel immédiat. Il consiste à demander à nouveau les mots de la liste que le patient devait mémoriser. Ces derniers peuvent être dits dans n’importe quel ordre. Un indice de catégorie doit être donné pour tous les mots dont le patient ne parvient pas à se rappeler.
Attention: Éviter de contaminer cette tâche en demandant au sujet de faire une autre tâche de mémoire verbale pendant le délai de 15 minutes!
Guide de passation
Administration: A) Une durée de 15 minutes doit s’être écoulée entre la fin du rappel immédiat et le début du rappel différé. L’examinateur donne les instructions suivantes: «Tout à l’heure, je vous ai fait lire une liste de mots que vous m’avez rappelé. Dites-moi tous les mots dont vous vous souvenez, dans n’importe quel ordre». L’examinateur encercle « L » pour tous les mots rappelés correctement. B) Pour tous les mots non-rappelés, l’examinateur donne les instructions suivantes: «Quel était le (nom de la catégorie)?». L’examinateur encercle « I » pour tous les mots rappelés à l’aide de l’indice de catégorie. C) Pour tous les mots non-rappelés, faites un X dans la colonne Ne sait pas. Lors du rappel différé, il est important de ne pas donner de rétroaction ou de bonne réponse au patient.
Cotation: Un point est alloué pour chaque mot rappelé librement ou avec un indice, et est noté dans la colonne appropriée.
Score total: 8
4. Reconnaissance
Une liste de mots, contenant les mots lus et mémorisés précédemment ainsi que de nouveaux mots (distracteurs), est lue au patient. Ce dernier doit alors dire, pour chaque mot, si ce dernier faisait partie de la liste ou non.
Guide de passation
Administration: L’examinateur dit: «Je vais vous lire une nouvelle liste de mots qui contient ceux que vous avez lus tout à l’heure, et de nouveaux mots. Pour chacun, dites "Oui" si c’est un mot de la liste que vous avez lue ou "Non" s’il s’agit d’un nouveau mot. Par exemple, si je vous dis Chemise, est-ce que ce mot était dans la liste, oui ou non ?» L’examinateur indique par un crochet la réponse du sujet (oui ou non). Lorsque le sujet identifie un mot qui n’était pas dans la liste de mot à mémoriser, l’administrateur doit cocher la case Faux positif.
Cotation: Un point est alloué pour chaque mot de la liste de mot correctement identifié. Un point est soustrait pour chaque mot ajouté à la liste de mot (faux positif).
Score total: 8
Index 2 – Visuospatial (score total de 7)
L’index visuospatial permet d’apprécier, par ses trois tests, la capacité du patient d’analyser et de se représenter l’espace.
1. Détection de formes
Ce test explore les habiletés visuoperceptuelles soit la capacité du patient d’intégrer les éléments visuels dans l’espace pour former un tout cohérent. Un dessin montrant des objets empilés les uns sur les autres, ne montrant que les contours de ces objets est présenté. Celui-ci doit alors nommer tous les objets qu’il lui est possible de voir sur l’image.
Guide de passation
Administration: A) L’examinateur présente la carte Détection de formes et donne les instructions suivantes: «Nommez tous les objets que vous voyez sur ce dessin». B) Si le sujet n’identifie pas tous les objets, l’administrateur donne les instructions suivantes: «Très bien, est-ce que vous voyez d'autres objets ?».
Cotation: Un demi-point est alloué pour chaque objet correctement identifié et un point est alloué lorsque le coffre est identifié.
Score total: 3
2. Rotation perceptuelle
Dans ce test, le sujet doit choisir parmi 4 choix l’image qui représente ce qu’il verrait s’il était situé à un point précis dans la scène. Ce test est composé de 2 scènes ayant pour thème la ferme, soit celle de la personne à vélo et celle du fermier.
Guide de passation
Administration: A) L’examinateur présente la carte de la ferme (vélo) et donne les instructions suivantes: «Si vous étiez à la place de cette personne à vélo (pointez la personne à vélo), laquelle des images suivantes (pointez les choix en bas) correspondrait le mieux à ce que vous verriez devant vous ?». L’examinateur note la réponse du sujet. B) L’examinateur présente la carte de la ferme (fermier) et donne les instructions suivantes: «Si vous étiez à la place du fermier (pointez le fermier), laquelle des images suivantes (pointez les choix en bas) correspondrait le mieux à ce que vous verriez devant vous ?». L’examinateur note la réponse du sujet.
Cotation : Un point est alloué pour chaque bonne réponse.
Score total: 2
3. Construction visuospatiale
Cette tâche explore la capacité du sujet à reproduire/construire de manière identique un dessin complexe dans l’espace.
Guide de passation
Administration: L’examinateur présente la carte construction visuospatiale, donne une feuille blanche au sujet (page 12 - Feuillet du participant) et dit: «Copiez cette figure pour que votre dessin soit semblable au mien». Le sujet ne peut tourner la figure.
Cotation: Deux points sont alloués lorsque le dessin du sujet est identique ou ne comporte qu’une seule erreur. Un point est alloué lorsque le dessin présente au maximum 2 erreurs. Aucun point n’est alloué lorsque le dessin présente 3 erreurs ou plus. Lorsque les briques ne sont pas toutes correctement recopiées une à une, ne comptabilisez qu’une erreur.
Score total: 2
Index 3 – Fonctions exécutives (score total de 10)
Cet index comprend 6 sous-tests qui permettent d’évaluer les fonctions exécutives.
1. Empan à rebours
Cette tâche est composée de 3 séries de chiffres que le patient doit répéter en sens inverse. Contrairement à l’empan direct (Index Mémoire), l’empan à rebours requiert que le sujet manipule de l’information en mémoire de travail, d’où sa composante exécutive.
Guide de passation
Administration: L’examinateur lit les séquences de chiffre au rythme d’un par seconde après avoir donné les instructions suivantes : «Je vais vous lire des chiffres, mais cette fois, je voudrais que vous les répétiez à l’envers. Par exemple, si je dis 1–6, vous diriez…?». Écrivez la réponse du sujet et cotez 0 ou 1. À la première erreur, arrêtez le test.
Cotation: Un point est alloué pour chaque séquence correctement répétée.
Score total: 3
2. Mois à rebours
Ce test consiste à demander au patient de nommer les mois de l’année à l’envers en commençant par le mois de décembre.
Guide de passation
Administration: L’examinateur dit: «Nommez les mois de l’année à l’envers en commençant par Décembre».
Cotation: Un point est alloué pour une réponse exacte, c’est-à-dire aucune erreur dans la séquence de Décembre à Janvier. Un patient qui corrige son erreur a tous ses points.
Score total: 1
3. Séquence graphique
La copie d’une séquence graphique complexe permet d’apprécier la capacité d’alterner d’un symbole à l’autre, une habileté frontale exécutive.
Guide de passation
Administration: L’examinateur présente la séquence graphique du Feuillet du participant et dit: «Copiez ce dessin pour qu'il soit semblable au mien». L’administrateur doit s’assurer que la séquence est reproduite dans l’espace sous le modèle (Page 13 du Cahier de l’examinateur - Feuillet du participant).
Cotation: Un point est alloué si la copie de la séquence est identique.
Score total: 1
4. Similitudes
Ce sous-test permet d’évaluer la capacité d’abstraction en demandant d’identifier la similitude entre deux mots à priori différents.
Guide de passation
Administration: L’examinateur demande au sujet le point commun entre deux mots en le formulant ainsi: A) «Qu’est-ce que avion et bateau ont en commun? En quoi sont-ils semblables?». Lorsque le sujet ne donne pas la réponse attendue, l’administrateur dit: «Pouvez-vous m’en dire plus ?». B) «Qu’est-ce que peinture et cinéma ont en commun? En quoi sont-ils semblables?». C) «Qu’est-ce que tremblement de terre et ouragan ont en commun? En quoi sont-ils semblables?».
Cotation:
A) Avion et bateau:
1 point = moyens de transport;
0.5 point = Moteur, vont vites, etc.
B) Peinture et cinéma:
1 point = arts;
0.5 point = loisirs, images, etc.
C) Tremblement de terre et ouragan:
1 point = catastrophes naturelles;
0.5 point = cataclysmes, séismes, etc.
*Accordez 0.5 point pour toute réponse adéquate selon votre bon jugement clinique.
Score total: 3
5. Fluidité verbale
En demandant au patient de nommer le plus grand nombre de mots commençant par une lettre en une minute, le test de la fluidité verbale permet d’explorer les capacités exécutives de recherche lexicale active.
Guide de passation
Administration: L’examinateur dit: «Dites-moi le plus grand nombre de mots que vous connaissez en une minute. Par exemple, avec la lettre B, vous pourriez me dire Banane, Bateau, etc. Ne dites pas de noms propres (ex. Boston, Benoit, etc.), ni le même mot avec une fin différente, comme Boire, Boirons, Boirez. Ok? Allons-y. Donnez-moi le plus grand nombre de mots que vous connaissez en une minute, et qui commencent par la lettre A. Allez-y.». L’examinateur démarre le chronomètre dès la fin du terme «Allez-y» et arrête le sujet après 60 secondes. L’examinateur doit noter tous les mots énoncés par le sujet dans les cases appropriées. Lorsque le sujet ne nomme plus de mots pendant plus de 5 secondes, l’examinateur dit: «Lâchez pas, n’importe quel mot qui commence par la lettre …!».
Cotation: Un point est alloué si le sujet énonce plus de 12 mots en 60 secondes.
Score total: 1
6. Stroop
Ce test est une adaptation du Stroop Victoria qui permet d’évaluer les fonctions exécutives, plus précisément la capacité d’inhibition. Cette adaptation est constituée de 3 sections, soit les points de couleurs, la lecture de mots et l’interférence. Seule la carte Interférence est scorée. Pour chaque section, le patient doit dire le plus rapidement possible la couleur, le mot ou la couleur des mots.
Guide de passation
a) Points de couleur
Administration: L’examinateur présente la carte points de couleurs et dit: Voici une feuille sur laquelle sont représentés des points de couleur. Nous allons commencer par la ligne d’exemple où je vais vous demander de nommer la couleur des points, de gauche à droite, le plus rapidement possible en évitant les erreurs. Êtes-vous prêt? Allez-y!». En cas d'erreur, deux autres essais peuvent être proposés. Si des erreurs sont produites au troisième essai, l’épreuve débute quand même.
Puis, l’examinateur dit: «Nous allons faire le même exercice à nouveau en commençant ici en haut à gauche (pointez le lieu de début du test), le plus rapidement possible. Êtes-vous prêts? Allez-y!».
Cotation: Aucun point n’est alloué.
B) Lecture des mots
Administration: L’examinateur présente la carte lecture de mots et dit: «Voici une feuille sur laquelle sont écrits des mots. Je vais vous demander de lire ces mots de gauche à droite, le plus rapidement possible en évitant les erreurs. Nous allons commencer par la ligne d'exemple. Êtes-vous prêt? Allez-y». En cas d'erreur, deux autres essais peuvent être proposés. Si des erreurs sont produites au troisième essai, l’épreuve débute quand même.
Puis, l’examinateur dit: «Nous allons faire le même exercice à nouveau en commençant ici en haut à gauche (pointez le lieu de début du test), le plus rapidement possible. Êtes-vous prêts? Allez-y!».
Cotation: Aucun point n’est alloué.
C) Interférence
Administration: L’examinateur présente la carte interférence et dit: «Voici une feuille sur laquelle sont écrits des mots. Par exemple, le mot jaune est écrit en bleu. Je vais vous demander de me dire la couleur dans laquelle le mot est écrit. Procédez de gauche à droite, le plus rapidement possible en évitant les erreurs. Nous allons commencer par la ligne d'exemple. Êtes-vous prêt? Allez-y». L’examinateur démarre le chronomètre dès la fin du terme «Allez-y» et arrête le sujet après 15 secondes. L’examinateur note le nombre de bonnes réponses en 15 secondes.
Cotation: Un point est alloué si le sujet donne 11 bonnes réponses ou plus en 15 secondes. Une erreur que le sujet corrige immédiatement compte pour une bonne réponse.
Score total: 1
Index 4 – Langage (score total de 33)
Cet index évalue plusieurs aspects clés du langage et de la parole (dénomination, écriture, construction grammaticale, compréhension, répétition, prosodie, etc.).
1. Description orale d’une scène
La description orale d’une scène permet d’apprécier la présence d’un manque du mot, d’une difficulté dans la construction grammaticale, dans la clarté et/ou la cohérence du langage, de paraphasies (lexicales ou sémantiques) et aussi de noter le débit verbal (à la recherche d’une distinction entre un trouble de la parole versus un trouble du langage).
Guide de passation
Administration: L’examinateur présente la carte du chalet et dit: «Racontez-moi une histoire à partir de cette scène». Il peut encourager le sujet à décrire la scène avec le plus de détails possibles en utilisant les formules suivantes: «Est-ce qu’il y a autre chose?» ou «Très bien, continuez». L’examinateur doit évaluer divers aspects du langage et de la parole (absent, léger, significatif) selon la grille prévue à cet effet.
Cotation: Si la performance est impeccable, accordez un point. S’il y a présence d’une légère dysphasie, accordez 0.5 point. Si l’anomalie dans le langage est significative (selon votre bon jugement clinique), n’accordez aucun point.
Score total: 6
2. Dénomination et écriture
À l’aide de la même image utilisée pour la Description orale d’une scène, on demande ici au patient de nommer puis d’écrire le nom de stimuli spécifiquement pointés par l’examinateur. Si le mot n’est pas donné correctement, l’indice sémantique, puis l’indice phonologique sont fournis au sujet.
Guide de passation
Administration: Sur la carte du chalet, l’examinateur pointe le premier item identifié dans le Cahier de l’examinateur, et dit «Comment appelle-t-on cela?». Si le mot n’a pas été nommé correctement, l’examinateur donne l’indice sémantique en disant: «C’est dans le ciel». Si le sujet ne trouve pas la bonne réponse, l’examinateur donne l’indice sémantique souligné. L’examinateur doit cocher la case appropriée en fonction de la réponse du sujet. Une fois que le mot est nommé correctement, l’examinateur demande au sujet de l’écrire à la page 13 du Guide clinique - Feuillet du participant à l’endroit approprié en disant: «Très bien, pouvez-vous me l’écrire ici?».
Cotation: Allouez 0.5 point pour chaque réponse fournie sans indice ou avec indice sémantique. Aucun point n’est alloué pour une réponse fournie grâce à l’indice phonologique. Allouez 0.5 point pour chaque réponse correctement écrite.
Score total: 10 (5 pour Dénomination et 5 pour Écriture)
3. Description écrite d’une scène
Une nouvelle carte image est présentée au patient. Il lui est alors demandé d’écrire une petite histoire de 2-3 phrases afin de décrire ce qu’il voit sur l’image. Ce test permet d’apprécier la construction grammaticale, la cohérence des idées et jusqu’à un certain point, la perception visuelle d’une scène.
Guide de passation
Administration: L’examinateur présente la carte accident et dit: «Écrivez-moi une petite histoire en deux ou trois phrases à partir de cette scène. Lorsque vous aurez terminé, j’aimerais que vous la lisiez à voix haute ». L’examinateur pointe les lignes au bas de la page 13 du Guide clinique - Feuillet du participant et demande au sujet de lire son texte afin de bien saisir le sens. L’examinateur évalue ensuite la présence et le degré de dysphasie dans le texte du sujet (absent, léger, significatif).
Cotation: Si la dysphasie est absente, accordez un point. Si elle est légère, accordez 0.5 point. N’accordez aucun point si la dysphasie est significative.
Score total: 3
4. Compréhension
Cette section est composée de 3 situations qui visent à explorer si le patient est capable d’associer une description à la bonne image.
Guide de passation
L’administrateur ne doit donner aucun indice à propos de l’image et ne doit pas pointer en sa direction. Il présente chaque carte selon les instructions plus bas.
a) Carte baseball
Administration: L’examinateur présente la carte baseball et dit: «Pointez l’image qui montre un garçon qui vient de frapper la balle».
b) Carte docteur
Administration: L’examinateur présente la carte docteur et dit: «Pointez l’image qui montre un docteur qui annonce une bonne nouvelle».
a) Carte avion
Administration: L’examinateur présente la carte avion et dit: «Pointez l’image qui montre un avion qui attend pour décoller, car les conditions météo sont mauvaises».
Cotation: Pour chaque carte, allouez un point si le sujet pointe la bonne image.
Score total: 3
5. Sémantique
Le sous-test sur la mémoire sémantique est composé de 5 cartes qui consistent à demander au patient de pointer le concept sémantique mentionné par l’examinateur. La fluidité sémantique fait aussi partie de ce sous-test. Elle consiste à demander au patient de nommer le plus grand nombre de mots d’une même catégorie (les animaux) en une minute.
Guide de passation
L’administrateur ne doit donner aucun indice sur l’image et ne doit pas pointer en sa direction. Il présente chaque carte et énonce l’instruction appropriée.
a) Carte planète
Administration: L’examinateur présente la carte planète et dit: «Pointez une planète».
b) Carte moyen de transport
Administration: L’examinateur présente la carte moyen de transport et dit: «Pointez un moyen de transport».
c) Carte sportif
Administration: L’examinateur présente la carte sportif et dit: «Pointez le sportif».
d) Carte archéologue
Administration: L’examinateur présente la carte archéologue et dit: «Pointez l’archéologue».
e) Carte escorter
Administration: L’examinateur présente la carte escorter et dit: «Pointez l’image qui signifie escorter».
Cotation: Pour chaque carte, allouez un point si le sujet pointe la bonne image.
f) Fluidité sémantique
Administration: L’examinateur dit: «Nous allons refaire l'exercice comme tantôt du plus grand nombre de mots en une minute. Cette fois-ci, vous allez me donner des mots qui font partie d'une catégorie, par exemple tous les légumes. Ok? Donnez-moi tous les noms d’animaux que vous connaissez en une minute. Êtes-vous prêt? Allez-y!» L’examinateur démarre le chronomètre dès la fin du terme « Allez-y » et arrête le sujet après 60 secondes. Il doit noter tous les mots énoncés par le sujet dans les cases appropriées. Lorsqu’un mot est nommé plus d’une fois, l’examinateur doit marquer le mot avec « P » (pour persévération). Lorsqu’un mot est nommé, mais qu’il ne correspond pas à la catégorie, l’examinateur doit indiquer « E » (pour erreur de règles). Le score total correspond au nombre de mots produits moins les persévérations et les erreurs de règles.
Cotation: Un point est alloué si le sujet nomme plus 18 mots en 60 secondes. Les grandes catégories (oiseaux, mammifères, poissons, etc.) ne sont pas acceptées.
Score total: 6
6. Répétition
La répétition de mots et surtout de phrases longues et complexes permet d’évaluer, entre autres, l’intégrité de la boucle phonologique.
Guide de passation
Administration: L’examinateur dit: «Je vais vous demander de répéter après moi des mots ou des phrases. D’accord? Répétez le mot voiture». L’examinateur fait répéter les cinq items inscrits dans le Cahier de l’examinateur.
Cotation: Allouez un point pour chaque mot ou phrase correctement répétée. La répétition doit être intégrale, exacte et sans aucune faille.
Score total: 5
Index 5 – Comportemental (score total de 20)
Cette section est composée de 10 questions et elle est réalisée à l’aide d’un proche aidant. Le comportement actuel ou les changements de comportement du patient sont questionnés afin de mettre en évidence certaines difficultés qui pourraient ou non avoir un lien avec un syndrome dégénératif.
Guide de passation
Administration: Cette section doit être complétée avec un proche aidant qui connaît bien le sujet. L’examinateur l’informe qu’il lui posera certaines questions sur le comportement de ce dernier. Afin de poser les questions qui se répondent par oui ou par non, l’examinateur doit dire: «Actuellement, est-ce que…» et lire chaque énoncé.
Cotation: Deux points sont alloués par question si la réponse à la question est non. Score total: Possibilité d’un score de 20, si la réponse est négative pour les 10 questions.
5. Validation et normes
Sujets
Des participants sains âgés entre 50 et 85 ans, canadiens et dont la langue maternelle est le français, ont été recrutés par l’entremise des patients fréquentant la Clinique Interdisciplinaire de Mémoire du CHU de Québec-Université Laval et/ou par des annonces publiques dans divers journaux, entre les mois d’avril 2014 et mai 2016.
Le consentement éclairé des participants, tout comme l’approbation du comité d’éthique, ont été obtenus au préalable. Les critères d’exclusion étaient : une histoire de traumatisme crânien modéré ou sévère, de délirium dans les 6 derniers mois, de chirurgie intracrânienne, de troubles neurologiques (sclérose en plaques, AVC), d’encéphalite ou de méningite ancienne. Également, ils étaient exclus s’ils avaient une condition médicale ou métabolique non-traitée, des antécédents psychiatriques chroniques, s’ils avaient reçu des traitements oncologiques cérébraux dans la dernière année, s’ils avaient des problèmes d’alcoolisme ou d’abus de substances, des problèmes visuels ou auditifs invalidants, s’ils prenaient des médicaments expérimentaux ou s’ils étaient inaptes ou analphabètes.
L’échantillon total était composé de 400 participants (voir Tableau 2) dont le score DCQ moyen était de 89.2±7.4. Les données normatives ont été établies à partir d’un sous échantillon de patients ayant un score ≥ 26 au MoCA (n=250) (voir Tableau 3). Afin d’assurer que l’échantillon normatif ne comporte que des sujets cognitivement sains, cette valeur seuil du MoCA a été adoptée, en conformité avec les études antérieures établissant les normes du MoCA (Nasreddine et al., 2005) et avec ce qui est généralement accepté comme valeur seuil dans la littérature (Smith et al., 2007; Larner, 2012). Le score DCQ moyen dans l’échantillon normatif était de 92.14±4.8.
Tableau 2. Caractéristiques sociodémographiques de l’échantillon total (N = 400)
| Moyenne | Écart type | |
|---|---|---|
| Âge (années) | 65,7 | 8,8 |
| Éducation (années) | 15,2 | 3,7 |
| Sexe | Fréquence | % | |
|---|---|---|---|
| Masculin | 214 | 46,5 | |
| Féminin | 186 | 3,7 |
Tableau 3. Caractéristiques sociodémographiques de l’échantillon normatif (n = 250)
| Décompte | % | |
|---|---|---|
| Âge (années) | 63,3 | 7,7 |
| Éducation (années) | 16 | 3,3 |
| Groupes d'âge (années) | Fréquence | % | |
|---|---|---|---|
| 50-49 | 84 | 33,6 | |
| 60-69 | 114 | 45,6 | |
| 70-79 | 45 | 18 | |
| 80-85 | 7 | 2,8 | |
| Sexe | Fréquence | % | |
| Masculin | 157 | 62,8 | |
| Féminin | 93 | 37,2 |
Matériel et procédure
Le DCQ a été développé à la Clinique Interdisciplinaire de Mémoire (CIME) du CHU de Québec-Université Laval par un groupe d’experts en neurologie comportementale, en orthophonie et neuropsychologie clinique. Le DCQ cible 5 domaines cognitifs : Mémoire, Visuospatial, Exécutif, Langage et Comportemental. Ce dernier index a été complété grâce à une entrevue avec un proche du participant. Tous les sujets ont complété deux tests, soit le DCQ (25 minutes) et le MoCA (20 minutes), dans un ordre aléatoire, le même jour. Les tests ont été administrés par des psychomotriciens ayant reçu une formation préalable. La corrélation entre le DCQ et le MoCA a été étudiée afin d’évaluer la validité. Un échantillon aléatoire de 45 individus a été retesté dans un délai de 1 à 3 mois afin d’évaluer la fiabilité test-retest. Cinquante tests ont été scorés par deux évaluateurs indépendants pour établir la fiabilité inter-juges.
Validité et fiabilité
Le coefficient de corrélation de Pearson entre le DCQ et le MoCA était significativement élevé (r=0.71, p<0.001) (voir figure 3). La consistance interne évaluée par le coefficient alpha de Cronbach était satisfaisante à 0.736. La fiabilité test-retest dans un délai moyen de 48.7±13.9 jours était acceptable, avec une corrélation de 0.7 (p<0.001). La fiabilité inter-juges était excellente (ICC=0.99, P<0.001).
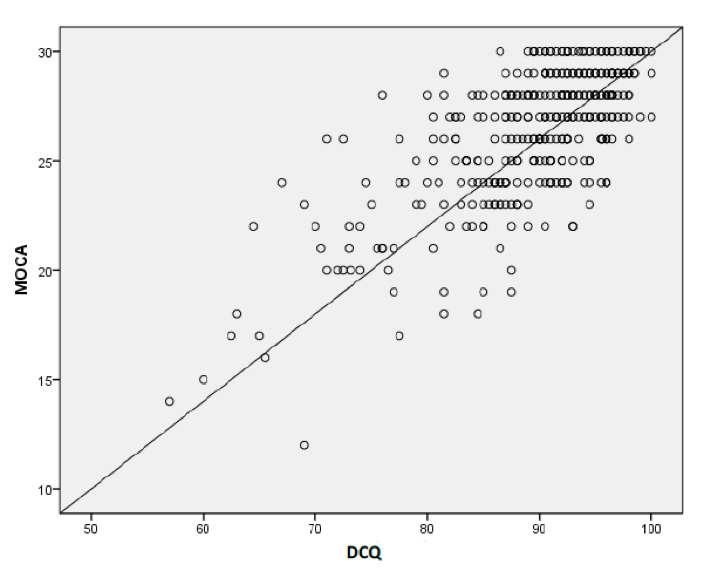
Figure 3. Corrélation entre le MoCA et le DCQ (score total)
Normes
Les normes établies dans un échantillon de 250 sujets ont été stratifiées selon l’âge et la scolarité (le niveau d’éducation a été divisé en deux groupes soit 12 et 12 ans de scolarité). Les données normatives, présentées en percentiles, sont fournies dans le Tableau 4. Elles incluent les rangs en percentiles, les groupes d’âges (50-59, 60-69, 70-79 et 80-85 ans) ainsi que le nombre de participants à l’étude dans chaque catégorie. Les normes pour les 5 index du DCQ sont présentées dans le Tableau 5. Afin de les utiliser, il suffit de sélectionner le groupe d’âge ainsi que le niveau d’éducation du patient et de se référer au rang centile correspondant. La médiane est le 50e percentile.
Tableau 4. Normes en percentiles pour le DCQ score total
| Âge | Éducation | n | Percentiles | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 5 | 10 | 15 | 25 | 50 | 75 | 85 | 90 | 95 | 8 | 99 | |||
| 50-59 | ≤12 | 12 | 86 | 86 | 86 | 86 | 88 | 90 | 93 | 94 | 98 | 98 | - | - | - |
| >12 | 72 | 76 | 77 | 83 | 87 | 89 | 92 | 94 | 96 | 98 | 98 | 99 | 100 | - | |
| 60-69 | ≤12 | 14 | 82 | 82 | 82 | 84 | 86 | 87 | 90 | 94 | 95 | 96 | - | - | - |
| >12 | 100 | 80 | 80 | 84 | 87 | 89 | 90 | 92 | 96 | 96 | 97 | 98 | 99 | 99 | |
| 70-79 | ≤12 | 14 | 81 | 81 | 81 | 81 | 81 | 86 | 88 | 92 | 92 | 93 | - | - | - |
| >12 | 31 | 71 | 71 | 74 | 83 | 87 | 89 | 91 | 94 | 95 | 96 | 97 | - | - | |
| 80-85 | ≤12 | 5 | 72 | 72 | 72 | 72 | 72 | 77 | 87 | 89 | - | - | - | - | - |
| >12 | 2 | 82 | 82 | 82 | 82 | 82 | 82 | 84 | - | - | - | - | - | - | |
Tableau 5. Normes en percentiles pour les cinq index du DCQ
| Index | Âge | Éducation | n | Percentiles | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 5 | 10 | 15 | 25 | 50 | 75 | 85 | 90 | 95 | 98 | 99 | ||||
| Mémoire | 50-59 | ≤12 | 12 | 27 | 27 | 27 | 27 | 27 | 28 | 28 | 29 | 30 | 30 | - | - | - |
| >12 | 77 | 25 | 25 | 26 | 27 | 27 | 28 | 29 | 30 | 30 | 30 | 30 | 30 | - | ||
| 60-69 | ≤12 | 16 | 26 | 26 | 26 | 26 | 26 | 27 | 28 | 29 | 30 | 30 | - | - | - | |
| >12 | 103 | 19 | 24 | 25 | 26 | 27 | 27 | 29 | 29 | 30 | 30 | 30 | 30 | 30 | ||
| 70-79 | ≤12 | 16 | 26 | 26 | 26 | 26 | 27 | 28 | 28 | 29 | 29 | 29 | - | - | - | |
| >12 | 32 | 21 | 21 | 22 | 24 | 25 | 27 | 27 | 29 | 29 | 29 | 30 | - | - | ||
| 80-85 | ≤12 | 5 | 24 | 24 | 24 | 24 | 24 | 24 | 24 | 29 | - | - | - | - | - | |
| >12 | 2 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | 25 | ||
| Visuospatial | 50-59 | ≤12 | 12 | 5 | 5 | 5 | 5 | 5 | 6 | 6 | 7 | 7 | 7 | - | - | - |
| >12 | 77 | 4 | 4 | 5 | 6 | 6 | 6 | 7 | 7 | 7 | 7 | 7 | 7 | - | ||
| 60-69 | ≤12 | 16 | 3 | 3 | 3 | 3 | 4 | 4 | 6 | 7 | 7 | 7 | - | - | - | |
| >12 | 103 | 4 | 5 | 5 | 5 | 6 | 6 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | ||
| 70-79 | ≤12 | 16 | 2 | 2 | 2 | 4 | 5 | 5 | 6 | 6 | 7 | 7 | - | - | - | |
| >12 | 32 | 3 | 3 | 3 | 4 | 5 | 5 | 6 | 7 | 7 | 7 | 7 | - | - | ||
| 80-85 | ≤12 | 5 | 5 | 5 | 5 | 5 | 5 | 5 | 5 | 6 | - | - | - | - | - | |
| >12 | 2 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | 7 | ||
| Exécutif | 50-59 | ≤12 | 12 | 6 | 6 | 6 | 6 | 6 | 6 | 8 | 9 | 10 | 10 | - | - | - |
| >12 | 77 | 4 | 5 | 5 | 6 | 7 | 8 | 9 | 9 | 10 | 10 | 10 | 10 | - | ||
| 60-69 | ≤12 | 16 | 5 | 5 | 5 | 5 | 6 | 6 | 7 | 8 | 9 | 10 | - | - | - | |
| >12 | 103 | 5 | 5 | 6 | 6 | 7 | 7 | 8 | 9 | 9 | 10 | 10 | 10 | 10 | ||
| 70-79 | ≤12 | 16 | 4 | 4 | 4 | 4 | 4 | 5 | 7 | 8 | 9 | 9 | - | - | - | |
| >12 | 32 | 4 | 4 | 4 | 6 | 6 | 6 | 8 | 9 | 9 | 9 | 9 | - | - | ||
| 80-85 | ≤12 | 5 | 4 | 4 | 4 | 4 | 4 | 5 | 6 | 8 | - | - | - | - | - | |
| >12 | 2 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | 6 | ||
| Langage | 50-59 | ≤12 | 12 | 28 | 28 | 28 | 28 | 28 | 29 | 30 | 31 | 32 | 32 | - | - | - |
| >12 | 77 | 28 | 28 | 29 | 30 | 31 | 31 | 32 | 32 | 32 | 33 | 33 | 33 | - | ||
| 60-69 | ≤12 | 16 | 27 | 27 | 27 | 27 | 28 | 29 | 30 | 31 | 32 | 32 | - | - | - | |
| >12 | 103 | 27 | 28 | 28 | 29 | 30 | 30 | 31 | 32 | 32 | 32 | 33 | 33 | 33 | ||
| 70-79 | ≤12 | 16 | 26 | 26 | 26 | 26 | 26 | 28 | 29 | 30 | 31 | 31 | - | - | - | |
| >12 | 32 | 25 | 25 | 26 | 28 | 29 | 29 | 31 | 32 | 32 | 32 | 32 | - | - | ||
| 80-85 | ≤12 | 5 | 21 | 21 | 21 | 21 | 21 | 25 | 29 | 30 | - | - | - | - | - | |
| >12 | 2 | 29 | 29 | 29 | 29 | 29 | 29 | 80 | - | - | - | - | - | - | ||
| Comportemental | 50-59 | ≤12 | 11 | 16 | 16 | 16 | 16 | 17 | 20 | 20 | 20 | 20 | 20 | - | - | - |
| >12 | 71 | 6 | 7 | 12 | 14 | 14 | 16 | 20 | 20 | 20 | 20 | 20 | 20 | - | ||
| 60-69 | ≤12 | 14 | 12 | 12 | 12 | 14 | 17 | 18 | 19 | 20 | 20 | 20 | - | - | - | |
| >12 | 99 | 10 | 12 | 12 | 14 | 16 | 16 | 20 | 20 | 20 | 20 | 20 | 20 | - | ||
| 70-79 | ≤12 | 14 | 10 | 10 | 10 | 13 | 16 | 16 | 18 | 20 | 20 | 20 | - | - | - | |
| >12 | 30 | 10 | 10 | 10 | 13 | 16 | 16 | 18 | 20 | 20 | 20 | - | - | - | ||
| 80-85 | ≤12 | 5 | 16 | 16 | 16 | 16 | 16 | 16 | 18 | 19 | - | - | - | - | - | |
| >12 | 2 | 14 | 14 | 14 | 14 | 14 | 14 | 16 | - | - | - | - | - | - | ||
6. Profils cognitifs et perles cliniques
Le DCQ est présentement en phase de validation auprès de diverses populations cliniques. Le profil clinique associé aux différentes variantes de la maladie d’Alzheimer et au spectre des démences frontotemporales sera disponible d’ici deux ans.
Voici quelques perles cliniques à retenir en ce qui concerne le DCQ.
1. La distinction entre le rappel libre et la reconnaissance en mémoire.
La capacité d’un sujet à se rappeler des mots dans un test de mémoire peut être évaluée de diverses façons. Par exemple, le rappel libre exige que le sujet fournisse les mots sur demande sans aucun indice (exemple: un examen à réponses courtes). Cette tâche est difficile et repose beaucoup sur les habiletés frontales exécutives. Par ailleurs, on peut demander au sujet de reconnaître une information en mémoire via un test de rappel indicé (on donne des indices, sémantiques par exemple) ou encore un test de reconnaissance (exemple: un examen à choix multiples). Cette habileté à reconnaître un stimulus en mémoire repose davantage sur l’encodage hippocampique.
Lorsque le rappel libre est diminué et que la reconnaissance en mémoire est faible on peut soupçonner une dysfonction dans le spectre de la maladie d’Alzheimer. Cette maladie touche en effet l’hippocampe. À l’inverse, lorsque le rappel libre est diminué, mais que la reconnaissance est relativement mieux préservée, on peut soupçonner une anomalie dans le spectre des troubles touchant les fonctions frontales exécutives (trouble cognitif vasculaire, maladies psychiatriques, démences frontotemporales).
Attention, cette distinction n’est pas absolue… Plusieurs patients Alzheimer maintiennent une certaine capacité de reconnaissance en mémoire. Certains cas de démences frontotemporales sont désorientés dans le temps et montrent une faible performance en reconnaissance…
2. Toujours évaluer l’orientation et les capacités attentionnelles de base
Le DCQ ne comprend pas de test d’orientation comme tel. Cette capacité est évaluée à l’aide des tests classiques de dépistage (MMSE ou MoCA) et doit être revue jours après jours, particulièrement chez les patients hospitalisés ou en CHSLD hors de leur milieu de vie habituel. L’attention de base (l’empan) fait partie de l’Index Mémoire.
L’orientation et l’attention peuvent fluctuer dans le temps auquel cas le clinicien doit soupçonner un délirium. Il est fortement déconseillé d’administrer un test de dépistage cognitif pendant qu’un patient est en délirium.
3. Gare à l’interférence
Une fois qu’un contenu verbal est administré au sujet, il faut éviter de fournir un autre contenu verbal dans l’intervalle entre l’administration des stimuli et le rappel libre. Le tout pourrait amener une interférence. L’exemple classique de ceci est le patient qui récupère le mot MONDE au MMSE, alors qu’on lui demande quels étaient les trois mots donnés plus tôt.
4. Administrer le DCQ dans l’ordre proposé
Il n’y a pas d’ordre prédéterminé dans le DCQ, mais si vous suivez l’ordre suggéré vous éviterez de causer de l’interférence entre les processus cognitifs évalués.
7. Perspectives futures
La recherche sur le vieillissement de la population et les déficits cognitifs et comportementaux qui s’y rattachent représente une priorité canadienne. Au long cours, le DCQ sera traduit en anglais et validé dans cette langue. Nous sommes également actuellement à dégager les profils de sensibilité et spécificité dans les variantes de la maladie d’Alzheimer (amnésique, visuelle, logopénique et frontale/dysexécutive), le spectre des démences frontotemporales (variante comportementale, le syndrome corticobasal, la paralysie supranucléaire progressive), le trouble cognitif vasculaire, et les maladies psychiatriques. La réponse des divers intervenants en santé (Ergothérapeutes, Neuropsychologues, Médecins) a été absolument incroyable et de nombreuses données feront l’objet de la version 2 du DCQ d’ici quelques années.
Ces travaux permettront aussi le développement d’un algorithme décisionnel utilisable par le clinicien de 1ière ligne. La finalité ultime sera d’améliorer l’identification précoce et le diagnostic différentiel des patients avec une démence typique et atypique. Diminuer le délai de prise en charge, instaurer le bon traitement sans délai, retarder l’institutionnalisation, diminuer les coûts sur le système de santé et la souffrance associée à ces maladies mal reconnues sont parmi les impacts majeurs et potentiels du DCQ.
8. Autres publications sur le DCQ
Laforce R.Jr, Sellami L, Bergeron D, Paradis A, Verret L, Fortin M-P, Houde M, Roy M, Poulin S, Macoir J, Hudon C, Bouchard R.W. Validation of the DCQ (Dépistage Cognitif de Québec): A new cognitive screening tool for atypical dementias. Archives of Clinical Neuropsychology (soumis).
Bergeron D, Roy M, Fortin MP, Houde M, Hudon C, Poulin S, Verret L, Bouchard RW, et Laforce R.Jr. Dépistage Cognitif De Québec (DCQ): A Novel Cognitive Screening Test for Atypical Dementias. Alzheimer’s & Dementia. Juil 2015; 11(7:Suppl):P568.
Laforce R.Jr, Bergeron D, Bouchard R.W, Fortin M-P, Houde M, Hudon C, Paradis A, Poulin S, Roy M, Vallières C, et Verret L. Validation du Dépistage Cognitif du Québec (DCQ), un outil de dépistage des démences atypiques. Communication présentée au 2e Congrès québécois sur la maladie d'Alzheimer. Québec, Québec, 5-7 novembre 2014.
Roy M, Laforce R.Jr, Poulin S, Verret L, et Bouchard R.W. Le Dépistage Cognitif de Québec (DCQ): vers un meilleur outil de dépistage des démences. Communication présentée au 1er Congrès québécois sur la maladie d'Alzheimer. Cahier des résumés, p.4, Montréal, Québec, 15-17 novembre 2012.
9. Références
Appels BA, Scherder E. The diagnostic accuracy of dementia-screening instruments with an administration time of 10 to 45 minutes for use in secondary care: a systematic review. Am J Alzheimers Dis Other Demen 2010; 25(4): 301-16.
Bergman H, Arcand M, Bureau C, Chertkow H, Ducharme F, Joanette Y. Relever le défi de la maladie d’Alzheimer et des maladies apparentées: une vision centrée sur la personne, l’humanisme et l’excellence—Rapport du comité d’experts en vue de l’élaboration d’un plan d’action pour la maladie d’Alzheimer.[Meeting the challenge of Alzheimer disease and related disorders: A vision centered on the person, humanism and excellence—Report by the committee of experts in view of developing an action plan for Alzheimer disease]. Ministère de la Santé et des Services sociaux; 2009.
Boeve BF, Graff-Radford NR. Cognitive and behavioral features of c9FTD/ALS. Alzheimers Res Ther 2012; 4(4): 29.
Dong Y, Sharma VK, Chan BP, Venketasubramanian N, Teoh HL, Seet RC, et al. The Montreal Cognitive Assessment (MoCA) is superior to the Mini-Mental State Examination (MMSE) for the detection of vascular cognitive impairment after acute stroke. J Neurol Sci 2010; 299(1-2): 15-8.
Folstein MF, Folstein SE, McHugh PR. "Mini-mental state". A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res 1975; 12(3): 189-98.
Frisoni GB, Pievani M, Testa C, Sabattoli F, Bresciani L, Bonetti M, et al. The topography of grey matter involvement in early and late onset Alzheimer's disease. Brain 2007; 130(Pt 3): 720-30.
Galton CJ, Patterson K, Xuereb JH, Hodges JR. Atypical and typical presentations of Alzheimer's disease: a clinical, neuropsychological, neuroimaging and pathological study of 13 cases. Brain 2000; 123 Pt 3: 484-98.
Gauthier S, McDowell I, Hill G. Canadian Study of Health and Aging (CaSHA). Psychiatr J Univ Ott 1990; 15(4): 227-9.
Gauthier S, Patterson C, Chertkow H, Gordon M, Herrmann N, Rockwood K, et al. Recommendations of the 4th Canadian Consensus Conference on the Diagnosis and Treatment of Dementia (CCCDTD4). Can Geriatr J 2012; 15(4): 120-6.
Geneau D, Taillefer D. PECPA - 2r : Protocole d'examen cognitif de la personne âgée. [cited; Available from: http://www.sepec.ca/pecpa.html
Gorelick PB, Scuteri A, Black SE, DeCarli C, Greenberg SM, Iadecola C, et al. Vascular contributions to cognitive impairment and dementia a statement for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2011; 42(9): 2672-713.
Gorno-Tempini ML, Dronkers NF, Rankin KP, Ogar JM, Phengrasamy L, Rosen HJ, et al. Cognition and anatomy in three variants of primary progressive aphasia. Ann Neurol 2004; 55(3): 335-46.
Gorno-Tempini ML, Hillis AE, Weintraub S, Kertesz A, Mendez M, Cappa SF, et al. Classification of primary progressive aphasia and its variants. Neurology 2011; 76(11): 1006-14.
Grossman M. The non-fluent/agrammatic variant of primary progressive aphasia. The Lancet Neurology 2012; 11(6): 545-55.
Hoops S, Nazem S, Siderowf AD, Duda JE, Xie SX, Stern MB, et al. Validity of the MoCA and MMSE in the detection of MCI and dementia in Parkinson disease. Neurology 2009; 73(21): 1738-45.
Hurd MD, Martorell P, Langa KM. Monetary costs of dementia in the United States. N Engl J Med 2013; 369(5): 489-90.
Josephs KA, Duffy JR, Strand EA, Machulda MM, Senjem ML, Master AV, et al. Characterizing a neurodegenerative syndrome: primary progressive apraxia of speech. Brain 2012: aws032.
Kelley BJ, Boeve BF, Josephs KA. Young-onset dementia: demographic and etiologic characteristics of 235 patients. Arch Neurol 2008; 65(11): 1502-8.
Knopman DS, DeKosky ST, Cummings JL, Chui H, Corey-Bloom J, Relkin N, et al. Practice parameter: diagnosis of dementia (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2001; 56(9): 1143-53.
Laforce RJ, Lehmann M, Macoir J, Poulin S, Roy M, Soucy JP, et al. Symptoms of Neurodegenerative Diseases. In: Saba L, editor. Imaging in Neurodegenerative Disorders. 1st ed: Oxford University Press; 2015. p. 592.
Laforce RJ, Sellami L, Bergeron D, Paradis A, Verret L, Fortin M-P, et al. Validation of the DCQ (Dépistage Cognitif de Québec): A new cognitive screening tool for atypical dementias (soumis). Archives of Clinical Neuropsycology.
Larner AJ. Screening utility of the Montreal Cognitive Assessment (MoCA): in place of--or as well as--the MMSE? Int Psychogeriatr 2012; 24(3): 391-6.
Lee SE, Rabinovici GD, Mayo MC, Wilson SM, Seeley WW, DeArmond SJ, et al. Clinicopathological correlations in corticobasal degeneration. Ann Neurol 2011; 70(2): 327-40.
Mahoney CJ, Downey LE, Ridgway GR, Beck J, Clegg S, Blair M, et al. Longitudinal neuroimaging and neuropsychological profiles of frontotemporal dementia with C9ORF72 expansions. Alzheimers Res Ther 2012; 4(5): 41.
McKeith I, Dickson DW, Lowe J, Emre M, O'brien J, Feldman H, et al. Diagnosis and management of dementia with Lewy bodies third report of the DLB consortium. Neurology 2005; 65(12): 1863-72.
McKhann GM, Knopman DS, Chertkow H, Hyman BT, Jack CR, Jr., Kawas CH, et al. The diagnosis of dementia due to Alzheimer's disease: recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease. Alzheimers Dement 2011; 7(3): 263-9.
Mendez MF, Joshi A, Tassniyom K, Teng E, Shapira JS. Clinicopathologic differences among patients with behavioral variant frontotemporal dementia. Neurology 2013; 80(6): 561-8.
Migliaccio R, Agosta F, Rascovsky K, Karydas A, Bonasera S, Rabinovici GD, et al. Clinical syndromes associated with posterior atrophy: early age at onset AD spectrum. Neurology 2009; 73(19): 1571-8.
Nasreddine ZS, Phillips NA, Bedirian V, Charbonneau S, Whitehead V, Collin I, et al. The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc 2005; 53(4): 695-9.
Nazem S, Siderowf AD, Duda JE, Have TT, Colcher A, Horn SS, et al. Montreal cognitive assessment performance in patients with Parkinson's disease with "normal" global cognition according to mini-mental state examination score. J Am Geriatr Soc 2009; 57(2): 304-8.
Ossenkoppele R, Pijnenburg YA, Perry DC, Cohn-Sheehy BI, Scheltens NM, Vogel JW, et al. The behavioural/dysexecutive variant of Alzheimer’s disease: clinical, neuroimaging and pathological features. Brain 2015; 138(9): 2732-49.
Petersen RC, Roberts RO, Knopman DS, Boeve BF, Geda YE, Ivnik RJ, et al. Mild cognitive impairment: ten years later. Arch Neurol 2009; 66(12): 1447-55.
Petersen RC, Thomas RG, Grundman M, Bennett D, Doody R, Ferris S, et al. Vitamin E and donepezil for the treatment of mild cognitive impairment. N Engl J Med 2005; 352(23): 2379-88.
Rabinovici GD, Miller BL. Frontotemporal lobar degeneration: epidemiology, pathophysiology, diagnosis and management. CNS Drugs 2010; 24(5): 375-98.
Rascovsky K, Hodges JR, Knopman D, Mendez MF, Kramer JH, Neuhaus J, et al. Sensitivity of revised diagnostic criteria for the behavioural variant of frontotemporal dementia. Brain 2011; 134(Pt 9): 2456-77.
Ratnavalli E, Brayne C, Dawson K, Hodges JR. The prevalence of frontotemporal dementia. Neurology 2002; 58(11): 1615-21.
Renner JA, Burns JM, Hou CE, McKeel DW, Jr., Storandt M, Morris JC. Progressive posterior cortical dysfunction: a clinicopathologic series. Neurology 2004; 63(7): 1175-80.
Rossor MN, Fox NC, Mummery CJ, Schott JM, Warren JD. The diagnosis of young-onset dementia. Lancet Neurol 2010; 9(8): 793-806.
Smith T, Gildeh N, Holmes C. The Montreal Cognitive Assessment: validity and utility in a memory clinic setting. Can J Psychiatry 2007; 52(5): 329-32.
Snowden JS, Harris J, Richardson A, Rollinson S, Thompson JC, Neary D, et al. Frontotemporal dementia with amyotrophic lateral sclerosis: a clinical comparison of patients with and without repeat expansions in C9orf72. Amyotroph Lateral Scler Frontotemporal Degener 2013; 14(3): 172-6.
Tabert MH, Manly JJ, Liu X, Pelton GH, Rosenblum S, Jacobs M, et al. Neuropsychological prediction of conversion to Alzheimer disease in patients with mild cognitive impairment. Arch Gen Psychiatry 2006; 63(8): 916-24.
Tang-Wai DF, Graff-Radford NR, Boeve BF, Dickson DW, Parisi JE, Crook R, et al. Clinical, genetic, and neuropathologic characteristics of posterior cortical atrophy. Neurology 2004; 63(7): 1168-74.
von Gunten A, Brull J, Kung A, Simms K, Taillefer D, Geneau D, et al. The "Protocole d'Examen Cognitif de la Personne Agee - Lausanne" (PECPA-L): a cognitive assessment tool for the French-speaking elderly in Switzerland. Eur Neurol 2006; 55(1): 22-30.
Wimo A, Prince MJ. Word Alzheimer Report 2010 : the globaleconomic impact of dementia: Alzheimer's Disease International; 2010.
Zanetti M, Ballabio C, Abbate C, Cutaia C, Vergani C, Bergamaschini L. Mild cognitive impairment subtypes and vascular dementia in community-dwelling elderly people: a 3-year follow-up study. J Am Geriatr Soc 2006; 54(4): 580-6.
10. Liste des tableaux et figures
Tableaux
Tableau 1. Les types de démences
Tableau 2. Caractéristiques sociodémographiques de l’échantillon total (N = 400)
Tableau 3. Caractéristiques sociodémographiques de l’échantillon normatif (n = 250)
Tableau 4. Normes en percentiles pour le DCQ score total
Tableau 5. Normes en percentiles pour les cinq index du DCQ
Figures
Figure 1. Résumé des index du DCQ
